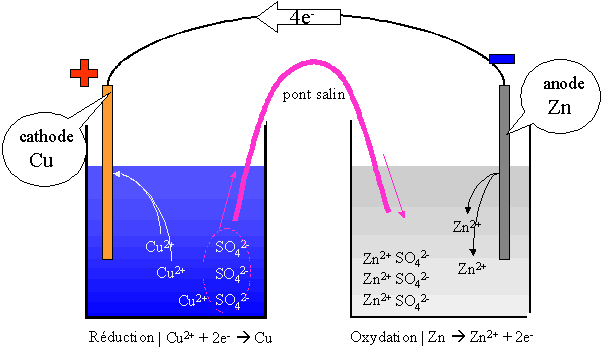
Deux couples sont en présence dans cette pile : Cu / Cu2+ (SO42-) et Zn / Zn2+ (SO42-). Le couple Cu/Cu2+ fera une réduction et le couple Zn/Zn2+ fera une oxydation.
l'oxydation se fait à l'anode (électrode négative) et la réduction se fait à la cathode (électrode positive).
Au départ, [Cu2+] = [SO42-] et [Zn2+] = [SO42-]
En fonctionnement, [Cu2+] < [SO42-] et [Zn2+] > [SO42-].
L'électrode de cuivre augmente de masse au cours du temps tandis que l'électrode de zinc va diminuer de masse au cours du temps.
Le pont salin va permettre aux ions SO42- de circuler d'un berlin à l'autre, afin que l'électro neutralité soit maintenue dans chacun des berlins. Ce pont est constitué soit d'un papier mouillé avec une solution d'un sel (NaCl, KCl, ...) soit d'un pont liquide constitué de la solution saline.
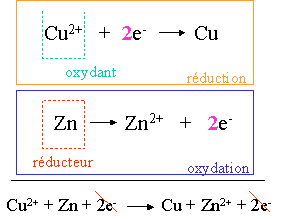
2023-01-29 02:01:00 / mazoughou@magoe.gn


0 commentaires
Votre impression compte aussi