Expérience :
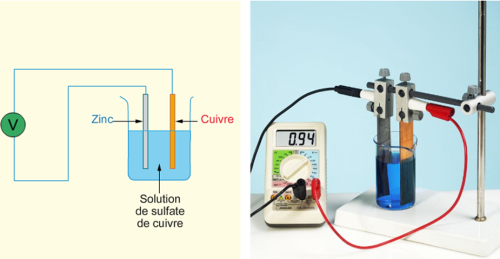
â–º On plonge deux lames métalliques (électrodes), l’une en cuivre et l’autre en zinc, dans un bécher contenant une solution de sulfate de cuivre.
â–º On relie les deux électrodes à un voltmètre.
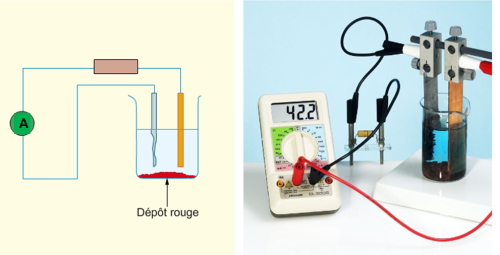
â–º On mesure ensuite l’intensité du courant débité par la pile après avoir inséré une résistance dans le circuit.
Observation :
Le voltmètre indique une tension d’environ 1V lorsque sa borne V est reliée à l’électrode de cuivre.
â–º L’ampèremètre indique une intensité d’environ 50 mA.
â–º L’électrode de zinc est rongée et du métal cuivre se dépose sur l’électrode de cuivre.
â–º La solution se décolore.
Interprétation :
L’électrode de cuivre constitue l’électrode positive de la pile et l’électrode de zinc constitue la borne négative.
La pile s’use :
â–º Du métal Zinc disparaît et des ions Zn2+ apparaissent.
â–º Des ions Cu2+ disparaissent et du métal cuivre se dépose sur l’électrode de cuivre.
Conclusion :
Une pile électrochimique est constituée de deux électrodes de natures différentes, généralement métalliques, plongeant dans un solution conductrice.
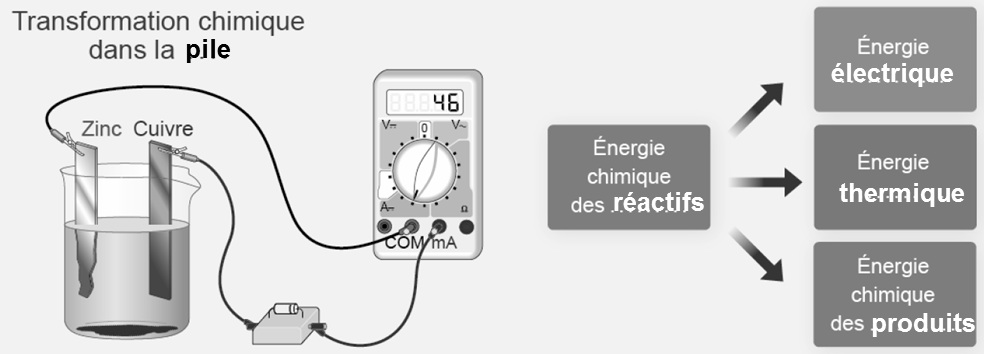
Lorsque la pile fonctionne, il se produit une transformation chimique (celle du paragraphe précédent).
Une partie de l’énergie chimique des réactifs est convertie en énergie électrique et une autre partie est transférée à l’extérieur sous forme d’énergie thermique .
La consommation des réactifs entraîne « l’usure »de la pile.
2020-06-14 20:59:08 / mazoughou@magoe.gn


0 commentaires
Votre impression compte aussi