Réaction d’oxydo-réduction avec transfert d’oxygène:
LA COMBUSTION DU CARBONE :
EXPERIENCE : le charbon du bois (c’est-à-dire pratiquement du carbone), chauffé au rouge dans l’air, plongé dans un flacon d’oxygène ; il brule avec une incandescence très vive.
Une fois la combustion est terminée, versons de l’eau de chaux dans le flacon et agitions après avoir fermé avec la paume de main, nous percevons une légère aspiration et l’eau de chaux se trouble.
Au cours de cette combustion qui dégage beaucoup de chaleur, l’oxygène du flacon et une partie du carbone disparaissent. Il se forme un gaz incolore qui se dissout dans l’eau et trouble l’eau de chaux. Dans ce cas, la solubilité dans l’eau et le trouble de l’eau sont les propriétés qui caractérisent le produit de cette combustion : le dioxyde de carbone.
C’est une réaction chimique dont l’équation bilan s’écrit.
Toutefois, il ne faut pas ignorer que, dans certaines conditions, la combustion du carbone dans l’air forme de monoxyde de carbone (CO), corps très toxique qui est l’origine de nombreux accidents mortels.
Activité 2 :
Réaliser et observer l’expérience de la combustion du soufre
LA COMBUSTION DU SOUFRE :
EXPERIENCE : le soufre enflammé dans l’air, brule avec une flamme bleue peu visible. Il se dégage un gaz irritant et toxique : le d’oxyde de soufre (SO2).
Lorsqu’il brûle dans le dioxygène, la flamme donnée par la combustion du soufre
est bien visible. Une fois la combustion est terminée :
- Versons de l’eau dans le flacon et agitons, après fermé avec la paume de
main nous percevons également une aspiration.
- Versons la solution du flacon dans une solution de permanganate de potassium (KMnO4), celle-ci est décolorée.
Au cours de cette combustion, l’oxygène du flacon et une partie du soufre disparaissent. Il se forme un gaz incolore et suffocant qui se dissout dans l’eau et décolore une solution de permanganate de potassium. Ces deux propriétés, solubilité dans l’eau et décoloration de la solution de permanganate de potassium caractérisent le produit de cette combustion : le dioxyde de soufre. L’équation bilan s’écrit :
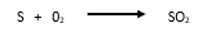
Notions que la combustion du soufre donne une petite quantité de trioxyde de soufre : SO3. Ce corps forme les fumées blanches peu solubles dans l’eau, que nous avons observées lors de la combustion du soufre.
LA COMBUSTION DU FER :
EXPERIENCE : la paille de fer fixée à l’extrémité d’un fil de fer brûle sans flamme à l’air et projette quelques étincelles.
Plongée dans un flacon d’oxygène, la paille de fer amorce la combustion du fil de fer qui brûle à son tour en dégageant beaucoup de chaleur, une partie du fer subit la fusion. Et il se forme un solide gris qui est l’oxyde magnétique ou du tétra oxyde de Fer de formule Fe3O4.
Équation bilan s’écrit :
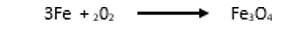
Définition de l’oxydoréduction:
Par transfert d’électrons, les termes suivants sont définis comme suit :
-
- Oxydation : C’est une réaction au cours de laquelle il y a perte d’électrons par un corps et qui s’accompagne d’une augmentation du degré d’oxydation
- Réduction : c’est une réaction au cours de laquelle il y a gain d’électrons par un corps et qui s’accompagne d’une diminution du degré d’oxydation.
- Oxydant : C’est toute espèce chimique (atome, ion, molécule,) capable de gagner un ou plusieurs électrons
- Réducteur : c’est toute espèce chimique (atome, ion, molécule) capable de perdre un ou plusieurs électrons.
- Oxydo-réduction : c’est une réaction au cours de laquelle il y a échange d’électrons entre un oxydant et un réducteur.
-
Oxydoréduction par voie sèche :
a) action du chlore sur le sodium : lorsqu’on fait brûler du sodium dans le chlorure de sodium. Ce solide a pour formule NaCl. L’équation – bilan qui résume cette réaction est :
-
Chaque petit cristal de chlorure de sodium formé contient un grand nombre d’ions sodium Na+ et le même nombre d’ions chlorure Cl-. Au cours de la réaction, chaque atome de sodium (Na) provenant du métal sodium a perdu un électron, on peut alors écrire la demi-équation électronique :
-
Simultanément, chaque molécule de dichlore en gagnant 2 électrons s’ionise
en ion chlore, on peut écrire la demi-équation électronique :
-
Au cours de cette réaction, le métal sodium se comporte en réducteur puis qu’il cède des électrons ; le gaz dichlore se comporte en oxydant puisqu’il gagne des électrons. La combustion du sodium dans le dichlore est donc une oxydoréduction.
REMARQUE : l’oxydoréduction par une sèche se distingue de celle dans l’électrolyse du fait que, l’oxydoréduction dans l’ectrolyse s’effectue en présence de l’eau, tandis que celle par voie sèche s’effectue en absence de l’eau.
1-3-4- OXYDOREDUCTION DANS L’ELECTROLYSE
Définition : l’électrolyse est l’ensemble des transformations chimiques qui se produisent quand le courant électrique traverse un électrolyte. Dans une électrolyse il y a oxydation à l’anobe (+) et réduction à la cathode (-).
-l’électrolyse de la solution de chlorure de sodium:
Lorsque le courant électrique passe dans la solution de chlorure de sodium, on observe la décomposition en ions.
Nous remarquons que, dans l’ectrolyse, l’oxydation et réduction sont simultanées ; mais elles se produisent séparément, l’une à l’anode, l’autre à la cathode. Nous remarquons en outre qu’elles sont inverses de celles qui interviennent dans la synthèse du chlorure de sodium
2024-05-16 15:34:48 / pascaline@magoe.gn


0 commentaires
Votre impression compte aussi