Les acides α-aminés constituent les matières de base des polypeptides et des protéines qui interviennent dans les systèmes de régulation et jouent le rôle d’enzymes (catalyseurs biologiques). Ce sont des molécules qui interagissent avec un milieu ayant un certain pH.
C’est le pH du milieu des acides aminés qui va déterminer leur forme ionique. En fait, les acides aminés ne sont jamais sous la forme NH2/COOH, mais plutôt sous trois types différents : la forme acide, la forme basique ou la forme isoélectrique, ou zwitterion.
Pour chaque acide aminé, il existe une valeur spécifique du pH où la charge globale de la molécule est nulle. Cette valeur de pH (pHi) représente le point isoélectrique où la concentration du zwitterion de l’acide aminé est maximale.
La charge globale portée par les différentes formes ioniques de l’acide aminé en solution dépend de la valeur du pH de la solution.
La charge électrique globale est nulle lorsque le pH de la solution est égal au pHi.
Elle est positive lorsque le pH de la solution est inférieur au pHi et négative lorsque le pH de la solution est supérieur au pHi.
1. ÉTUDE D’ACIDES AMINÉS
La glycine, ou acide 2-amino éthanoïque, et l’alanine sont les acides α-aminés les plus simples.
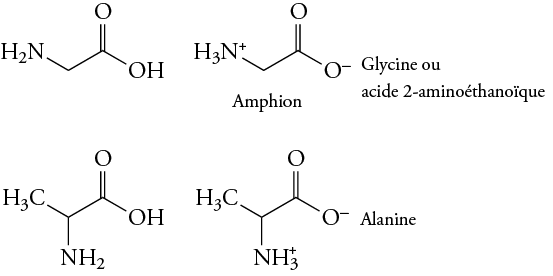
1.1. Identification des groupes caractéristiques
- Identifier les groupes caractéristiques présents sur ces deux molécules.
- Représenter l’alanine de façon à mettre en évidence le carbone asymétrique. Combien existe-t-il de stéréoisomères de l’alanine.
- Préciser leur nature.
- Qu’en est-il de la glycine ?
1.2. En solution aqueuse, il se forme presque exclusivement un ion dipolaire, appelé amphion ou zwitterion (représenté dans le tableau précédent).
- Définir un acide et une base selon Brønsted.
- Quel est l’acide conjugué de cet amphion (on donne pKA1 = 9,9) ?
- Écrire alors l’équation de la réaction de cet amphion avec l’eau.
- Quel est ici le rôle de l’eau ? Celui de l’amphion ?
- Quelle est la base conjuguée de cet amphion (on donne pKA2 = 2,3) ?
- Écrire alors l’équation de la réaction de cet amphion avec l’eau.
- Quel est ici le rôle de l’eau et celui de l’amphion ?
- Comment peut-on qualifier cet amphion ?
1.3 Les valeurs respectives des pKA des couples acido-basiques sont pKA1 = 2,3 et pKA2 = 9,9.
- Sur un axe de pH, indiquer les domaines de prédominance de chaque couple de l’alanine.
- On acidifie la solution aqueuse de l’alanine, on obtient un pH de 2. Quelle est l’espèce majoritaire ? Que se passe-t-il si la solution a un pH = 6, un pH = 11 ?
2. PRINCIPE DE L’ÉLECTROPHORÈSE
Des particules ayant une charge électrique et soumises à l’action d’un champ électrique se déplacent dans la direction du champ vers le pôle de signe opposé à leur charge, à une vitesse proportionnelle à cette charge.
On cherche à séparer par électrophorèse sur papier les acides aminés d’un mélange de proline (pHi = 6,3), de lysine (pHi = 9,7) et d’acide aspartique (pHi = 3) dont les formules semi-développées sont présentées ci-dessous.
On réalise cette expérience dans une solution tampon de pH = 6,3.
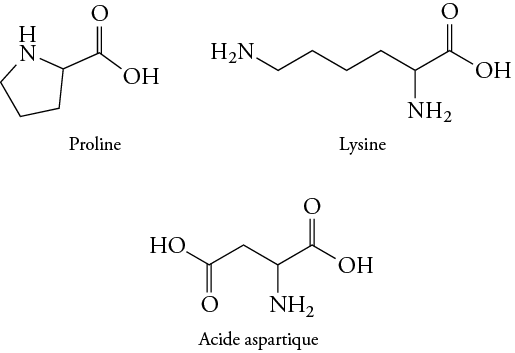
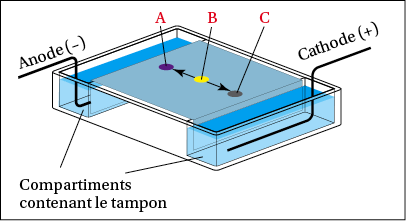
Le mélange est déposé au centre du papier. Les deux extrémités sont au contact d’un compartiment contenant une solution tampon. Chaque compartiment est relié à une électrode. Un générateur applique une tension pendant une heure.
Ensuite, on vaporise le papier avec de la ninhydrine, ce qui permet de révéler la présence des acides aminés par l’apparition de taches colorées.
- Quelle est la charge d’un acide aminé quand le pH de la solution est inférieur à son pHi ? Et quand il est supérieur au pHi ?
- Attribuer chaque tache obtenue ci-contre à un acide aminé en justifiant la réponse.
- Qu’est ce qu’une solution tampon ? Quel est l’intérêt d’utiliser une telle solution ?
- Le résultat aurait-il été identique si la solution tampon utilisée avait eu un pH de 10 ?
Guide
Partie 1
- 1.2. Repérer un carbone asymétrique est nécessaire pour identifier les stéréoisomères.
- 3. Le diagramme de prédominance permet de visualiser l’espèce qui est la plus présente à un pH donné, et l’espèce qui prédomine.
Partie 2
- 1. Le pHi n’est pas une connaissance du cours donc il faut aller rechercher sa particularité dans l’énoncé.
- Le papier sur lequel sont déposés les échantillons est imbibé de la solution tampon.
- 3. Une solution tampon est une solution dont le pH ne varie quasiment pas même avec un ajout d’acide, de base ou d’une solution faiblement diluée.


0 commentaires
Votre impression compte aussi