- Technique de dosage
- Rincer la burette avec la solution de soude. Ajuster le niveau de la soude à zéro.
- Rincer la pipette à l’acide et le bécher à l’eau cristallisée. Verser avec la pipette un volume VA d’acide à doser (généralement 10 ml ou 20 ml) y ajouter de BBT.
- Si l’on utilise aussi un pH-mètre, on ajoutera de l’eau distillée afin que les électrodes puissent tremper suffisamment on notera que cet ajout ne modifie pas la quantité d’ion H3O+déjà introduit.
- Faire un premier dosage rapide cm3 par cm3 afin de préparer la zone de virage agité en permanence.
- Faire un second dosage avec un niveau prélèvement d’acide versé alors la seule goutte à goutte dans la zone de virage repérée.
Noter le volume VB de solution de soude versé correspondant à la goutte qui provoque le virage de l’indicateur.
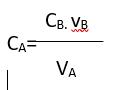
La concentration de l’acide est donné par
Indentification des ions :
- Méthodes d’identification des ions :
Il existe trois méthodes qui nous permettent d’identifier les ions :
- Couleurs spécifiques de certains ions.
Certains ions facilement identifiables à la couleur caractéristique.
Ex :
- L’ion permanganate MnO4- aq : violet
- L’ion bichromate Cr2O72- aq : orange.
- L’ion cuivre II Cu2+ aq : bleu
- L’ion fer II Fe2+ aq : vert pâle
- L’ion fer III Fe3+ aq : orange rouille.
- Test à la flamme
Certains ions portes dans une flamme d’un bee bunsen colorent la flamme avec une couleur caractéristique.
Ex :
- L’ion cuivre II : vert
- L’ion sodium : Na+ jaune – rouge.
- L’ion strontium : Sr2+ : rouge
- L’ion baryum : Ba2+ : rouge
- L’ion lithium Li+ : rouge
- L’ion plomb pb2+ : bleu pâle
- L’ion calcium Ca2+ : rouge orange
- Reaction de précipitation :
Certains composés ioniques sont solubles dans l’eau.
Ex : La dissolution du chlorure de sodium solide :
NaCl (s)  Na+ aq + Cl- aq
Na+ aq + Cl- aq
En revanche d’autres corps sont peu solubles dans l’eau.
Ex : Le chlorure d’argent AgCl ne dissout pratiquement pas dans l’eau.
- Tests d’identification des anions.
- L’ion sulfate : SO42-
Le test d’identification des ions SO42- est la formation du précipité blanc de sulfate de baryum BaSO4 par action de sulfate de sodium Na2SO4 sur une solution de nitrate de baryum.
(2Na+ + SO42-) + (Ba2+ + 2Na-3)  BaSO4 + 2Na+ 2Na3 soit
BaSO4 + 2Na+ 2Na3 soit
SO42- + Ba2+  BaSO4
BaSO4
- L’ion chlorure Cl-
Le test d’identification de l’ion chlorure Cl- est la formation d’un précipité blanc de chlorure d’argent (qui noircit progressivement AgNO3.
(Na + + Cl-) + (Ag+ + NO3-)  AgCl + Na+ +NO3-
AgCl + Na+ +NO3-
Autrement dit Cl- + Ag+  AgCl
AgCl
- L’ion sulfate : S2-
Il existe deux tests permettant de mettre en évidence l’ion S2-
- Premier test : dans une solution de sulfate de chlorhydrique. Il se produit immédiatement un dégagement gazeux de sulfate d’hydrogène.
(2Na+ + S2-)+ 2(H3O+ + Cl-)  H2S-2+2H2O + 2Na+ + 2Cl-
H2S-2+2H2O + 2Na+ + 2Cl-
S2- + 2H3O+  H2S-2 + 2H2O
H2S-2 + 2H2O
- Deuxième test : Dans une solution de sulfure de sodium on ajoute une solution de nitrate de plomb.
Il apparaît un précipité noir de sulfure de sulfure de plomb (Pbs)
(2Na+ + S-) + (Pb2+ + 2NO3-)  Pbs + 2Na+ + 2NO3- soit S2- + Pb 2+
Pbs + 2Na+ + 2NO3- soit S2- + Pb 2+ Pbs
Pbs
- L’ion carbonate : CO32-
On identifie l’ion carbonate en solution soit en ajoutant de l’eau de chaux sur le carbonate de sodium, il apparait un précipité blanc de carbonate de calcium
(2Na+ + CO2-3) + (Ca 2+ + 2OH) CaCO3 + 2Na + 2OH.
CaCO3 + 2Na + 2OH.
En faisant disparaître les ions spectateurs on aura Ca2+ + CO32-  CaCO3
CaCO3
- Soit en ajoutant de l’acide sulfurique sur le carbonate de sodium qui donne naissance à du dioxyde de carbone que l’on caractérise par la trouble qu’il produit avec l’eau de chaux.
(2Na+ CO32-) + ( H3O+ + SO42-)  CO2 + 3H2O.
CO2 + 3H2O.
CO32- + H3O+  CO2 + 3H2O.
CO2 + 3H2O.
- L’ions nitrate (NO3-)
Le test d’identification de l’ion nitrate NO3- en solution et l’apparition d’un gaz roux quand on ajoute du cuivre, metal et de l’acide sulfurique.
- Tests d’identification des cations :
- Les cations colorés : Dans certains cas la couleur de la solution suffit
Pour pouvoir affirmer la présence d’un cation à condition toute fois que cette solution sont bien marqué.
Il est possible de confirmer. Cette présence en ajoutant une solution d’hydroxyde de sodium de façon à faire précipitation les hydroxydes correspondants :
Fe2+ + 2OH-  Fe(OH)2 Hydroxyde de fer
Fe(OH)2 Hydroxyde de fer
II : précipité vert.
Fe2+ + 3OH-  Fe(OH)3 Hydroxyde de fer
Fe(OH)3 Hydroxyde de fer
III : Précipité rouille.
Cu2+ + 2OH  Cu (OH) Hydroxyde de cuivre
Cu (OH) Hydroxyde de cuivre
II : Précipité bleu.
Les cations Fe2+, Fe3+, Cu2+, se caractérisent par la couleur de leur solution aqueuse ou par leurs précipités d’hydroxyde.
- Les cations incolorés
- L’ion baryum : Ba2+ :
Le test d’identification de l’ion baryum Ba2+ est l’apparition d’un précipité blanc le sulfate de baryum quand on ajoute une solution d’ion sulfate
(Ba2+ + 2NO3-) + (Na 2+ + SO42-) BaSO4 + Na+ + 2NO3-
BaSO4 + Na+ + 2NO3-
Ba2+ + SO42-  BaSO4
BaSO4
- L’ion argent Ag+ : le test d’identification de l’ion argent Ag+ est l’apparition d’un précipité blanc de chlorure d’argent (noircissant à la lumière) quand on ajoute une solution d’ion chlorure.
(Ag+ + NO3-) + (Na+ + CL-)  AgCl précipité blanc.
AgCl précipité blanc.
- L’ion plomb : Pb2+
Le test d’identification de l’ion plomb Pb2+ est la formation d’un précipité noir de sulfure de plomb (Pbs) quand on goute une solution de sulfure.
(Pb2+ + 2NO3-) + (2Na+ + S)  Pbs + 2Na+ + 2NO3 ou encore
Pbs + 2Na+ + 2NO3 ou encore
Pb2+ + S2-  Pbs ( Précipité noir)
Pbs ( Précipité noir)
- L’ion Aluminium
Al3+ Le test d’identification de l’ion Al3+ est la formation d’un précipité blanc Al(OH) 3 quand on ajoute une solution diluée d’hydroxyde de sodium
(Al3+ + 2SO42-) + (3Na+ + 3OH)  Al(OH-)3 + Na+ + 2SO42- ou encore
Al(OH-)3 + Na+ + 2SO42- ou encore
Al3+ + 3OH- Al(OH-)3 Précipité
Al(OH-)3 Précipité
- L’ion Zinc : Zn2+
Le test d’identification de l’ion zinc est la formation d’un précipité blanc d’hydroxyde de zinc quand on ajoute une solution diluée d’hydroxyde de sodium (Zn2+ + SO42-) + (2Na+ + 2OH-) Zn(OH-) + 2Na+ + SO42- autrement
Zn(OH-) + 2Na+ + SO42- autrement
Zn2+ + 2OH  Zn(OH)2 blanc
Zn(OH)2 blanc
2020-05-22 18:25:29 / beavogui.gn@magoe.gn


0 commentaires
Votre impression compte aussi